1前言
本文研究流感病毒裂解疫苗(Fluavax),该疫苗来自CLS公司(澳大利亚),通过实验观察该疫苗的临床安全性以及该疫苗的免疫效果[1]。本次实验对象选择广西崇左市,并根据研究结果对该疫苗进行评价。
1.1 一般资料
通过初步检测筛查,选择确定符合临床标准的志愿者。具体如下表1-1。
表1-1 志愿者年龄分组
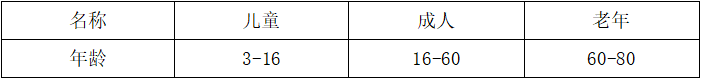
1.2 疫苗选择
1.2.1试验疫苗
流行性感冒病毒裂解疫苗(Fluavax),生产批号CTSLCHF0625A,由澳大利亚CLS公司生产。
1.2.2对照疫苗
对照组选用的疫苗名称为福禄立适(Fluarix)流感裂解疫苗,批号XFLUA207AA,由英国GSK公司生产。
1.3 接种效果观察
(1)在接种后,观察记录志愿者是否发生局部和全身反应。
(2)观察志愿者是否有免疫原性。
(3)疫苗的安全性要符合我国判断标准并根据标准进行分类[2]。详见下表1-2。
(4)免疫原性需要符合欧盟标准[3]
2 研究结果
2.1临床安全性研究
2.1.1临床反应观察
本次接种疫苗共690人,具体见下表2-1。所有志愿者接种剂量为1剂,观察他们的临床反应,均没有得到即时反应的接种者[4]。
表2-1 接种者各组人数
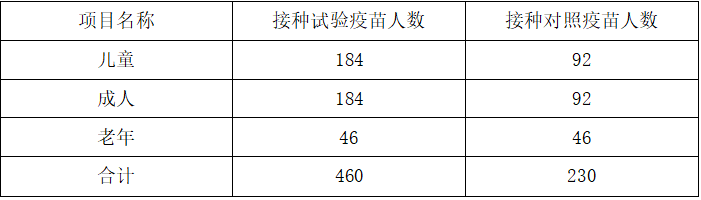
通过72h的观察记录后,有部分接种者出现全身反应,试验疫苗反应率4.13%,对照疫苗反应率为5.22%。
2.1.2 局部反应观察
通过统计,接种试验疫苗组出现局部反应共有19人,即局部发生率为4.13%,轻度发生率84.21%,中度发生率10.53%,重度发生率5.26%。具体见表2-3。
表2-3 接种试验疫苗局部反应情况
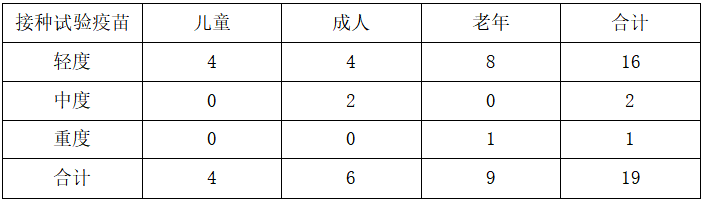
通过统计,接种对照疫苗组出现局部反应共有8人,局部发生率为3.48%,无发生中度及重度的局部反应。
2.2免疫原性研究
通过统计,有效双份血清样本共610对,占比88.41%,试验组有效样本87.61%,对照组有效样本90%。具体样本详见下表2-5。
表2-5 接种对照疫苗局部反应情况

2.2.1 两种流感疫苗免疫后HI抗体阳转率比较
试验组和对照组具体情况详见下表2-6。
表2-6 血清HI抗体阳转率情况
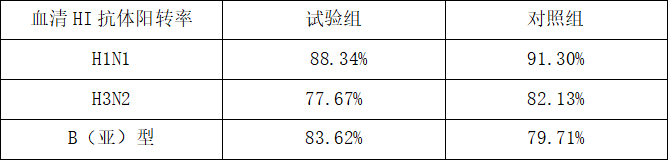
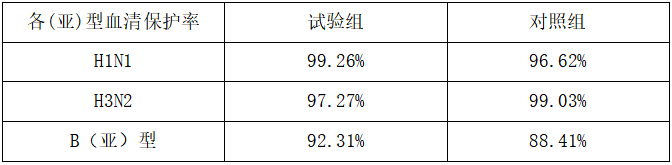
2.2.2两种流感疫苗免疫后血清保护率的比较
试验组和对照组具体情况详见下表2-7
表2-7 血清HI抗体阳转率情况
3 讨论
本次接种结果显示两家公司生产的疫苗出现反应率不高,试验组全身及局部反应率分别为4.13%和4.13%,对照组全身及局部反应率分别为5.22%和3.48%,差异很小且几乎48h之内已消退,说明两种疫苗有很高的安全性。
两种疫苗分别接种试验组和对照组后,研究结果显示,HI抗体总阳转率>40%,血清保护率>70%,免疫原性非常好。
综上,CSL有限公司生产的疫苗,符合欧盟标准,安全性、免疫原性非常好,可以大力推广使用。
参考文献
[1]戚凤春.流感疫苗的研究进展.中国生物制品学杂志,2004,17(3):190-192.[2]迮文远.预防接种手册.上海:上海科学技术文献出版社,1997,14-22.[3] 胡月梅,方捍华,高桂华,等.进口加拿大流行性感冒裂解疫苗临床安全性与免疫原性评价.中华流行病学杂志,2005,26(7):503-506.
[4]耿贯一.流行病学,第2版.北京:人民卫生出版社,1997,458.
致谢
在老师对我的指导和严格要求下,完成本篇论文。非常感谢老师的敦敦教导。




