一、电化学在高考中的考查
电化学是具有实用性的科学原理,其基本理论在高考中占有非常重要的地位,每年高考题都有对这部分内容的考查。主要考查知识的基础性、综合性、应用性和创新性,对学生独立思考、逻辑推理、信息加工等能力要求较高,大多数学生对这类试题感到迷茫。[1]电极反应式的书写是高中学生学习化学的一个很大障碍点,由于很多学生所接受到的关于电极反应式书写的信息比较混乱,因此,在书写电极反应式时感到无所适从。[2]如何较快较准解答电化学题型,需要我们化学教师去思考。经过对近几年全国高考理综化学试卷的研究和结合笔者多年的教学工作经验,发现学生在解答此类题目时尤其不会书写电极反应式。
二、电极反应式书写技巧
(一)关于燃料电池
燃料电池通常是正极通入氧气、负极通入可燃物,以惰性电极为电极材料的电池。若要书写正极电极反应式,则需分析电解质导电的实质及其酸碱性。例如:以碱性KOH溶液做介质的燃料电池,正极反应式:O2 + 4e- + 2H2O = 4OHˉ ;如果将电解质改为酸性介质,则正极又为O2+4H++4eˉ =2H2O;如果电解质换做熔融的固体氧化物,则正极反应又写为 O2+4eˉ =2O2ˉ;若电解质是熔融的K2CO3,同时正极还通入CO2气体,则又可写为2CO2+O2+4eˉ =2CO32ˉ
与之相对应的负极上的可燃物会发生失电子的氧化反应。无机可燃物可按基本方法计算化合价变化总数得出失电子数;对于含碳的、价态较多的有机物,计算化合价相对较费时间。要迅速书写电极反应式,可按照分析有机物被氧化是完全氧化还是部分氧化的方法做题。
1、有机物被完全氧化书写技巧:
失电子数目可以按照可燃物中元素:一般是含C、H、O,也可能含N等其他元素,可按有机物中元素化合价归零法判断化合价变化总数从而得出复杂有机物失电子数。若有机物中碳被完全氧化成+4价碳的化合物,则失电子数用“碳4氢1氧减2”来计算,(有氮等其他元素的存在时直接忽略。)
电极反应式切忌盲目书写,还需分析介质传导何种离子,传导离子能否和电极材料上物质或离子发生反应。可借助口诀“缺啥补啥看介质;介质两极分两端;离子分布想反应;若要配平用守恒”进行电极反应式的书写和选项中电极反应式的正误判断。
2、有机物被部分氧化书写技巧
例如:将反应2CH2=CH2+ O2→2CH3CHO 设计为燃料电池,如要书写负极电极反应式,则失电子数既可按正极O2得电子数目判断,又可按“部分氧化看氢氧;变化总和算电子;其他元素不用管”这个口诀来做题。分析得出,由CH2=CH2到CH3CHO的转变,相对CH2=CH2来说,CH3CHO只多了一个氧原子。那么转移的电子数就是2×1=2。这样就可以迅速写出该电极的负极反应式:举例碱性介质中为CH2=CH2-2eˉ + 2OH-→CH3CHO+ H2O
高考真题(2021全国甲卷第13题):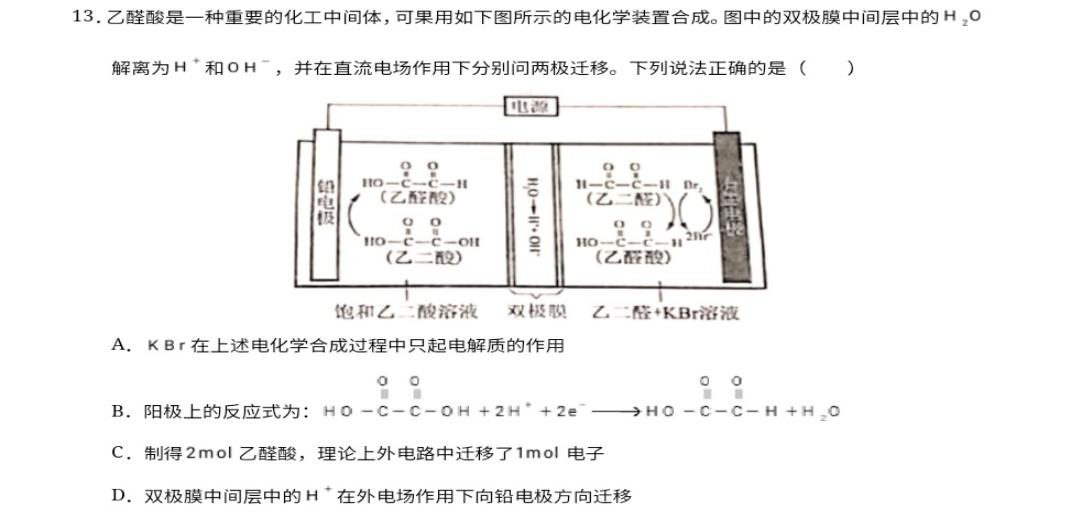 解析:此题的A选项错误,由溴离子到溴单质的相互转化证明溴化钾参与了阳极上的电极反应,而溴单质是阳极的中间产物;B、C选项需要书写电极反应式。可由箭头指向发现由乙二酸到乙醛酸的反应是失去氧的还原反应,化合价降低。则左侧铅电极是阴极,连接电源的负极。B改为阴极上的反应;C选项根据两电极反应式发现阴极和阳极均生成1mol乙醛酸,即制得2mol乙醛酸时理论上外电路迁移了2mol电子,C项错误;D项利用电解池离子移动“阴阳相吸”口诀得出结论D项正确。
解析:此题的A选项错误,由溴离子到溴单质的相互转化证明溴化钾参与了阳极上的电极反应,而溴单质是阳极的中间产物;B、C选项需要书写电极反应式。可由箭头指向发现由乙二酸到乙醛酸的反应是失去氧的还原反应,化合价降低。则左侧铅电极是阴极,连接电源的负极。B改为阴极上的反应;C选项根据两电极反应式发现阴极和阳极均生成1mol乙醛酸,即制得2mol乙醛酸时理论上外电路迁移了2mol电子,C项错误;D项利用电解池离子移动“阴阳相吸”口诀得出结论D项正确。
对于此类方程式书写还需快速配平,可以结合化学解题中的“守恒思想”配平:先配物质;再配电子(可以按照以上方法算出得失电子数目:B项阴极反应:氧原子数少了1而氢原子数未少,转移电子数2×1+0×1=2);配完电子配电荷(应用几个电子子几个酸快速配出氢离子及其数目);最后再结合化学守恒思想配平原子数目。
(二)关于一些复杂的电池反应
近年来锂离子电池考点相对比较复杂。锂离子电池是由锂电池发展而来的。目前考题中的锂离子电池为锂二次电池。【4】做此类题目也无需耗费太多时间计算元素化合价,而是分析锂离子移动方向。即放电时正电荷靠近的电极就是原电池的正极,(因为原电池离子移动可用“阳正阴负”四个字概括)。
例如关于锂的二次电池: Li1-xCoO2+LixC6 ![]() LiCoO2+6C 首先,我们可依照之前提到的方法迅速判断正负极。上述反应,左侧物质是放电时的反应物我们不难判断出带正电荷的锂离子是移到了 Li1-xCoO2的一极, (因为相对于该物质,右侧中锂离子增加了x个)。正极电极反应式为: Li1-xCoO2+xLi++xe-=LiCoO2。而该反应负极电极反应式为 LixC6 -xe- =xLi++6C , 由此可得 Li+由负极脱出迁向正极。类似的还有很多。
LiCoO2+6C 首先,我们可依照之前提到的方法迅速判断正负极。上述反应,左侧物质是放电时的反应物我们不难判断出带正电荷的锂离子是移到了 Li1-xCoO2的一极, (因为相对于该物质,右侧中锂离子增加了x个)。正极电极反应式为: Li1-xCoO2+xLi++xe-=LiCoO2。而该反应负极电极反应式为 LixC6 -xe- =xLi++6C , 由此可得 Li+由负极脱出迁向正极。类似的还有很多。
三、对教师讲解电化学题型的建议
基于学生在解答电化学题型时存在困惑的实际问题,建议教师在讲解完基本理论知识后,可采取以下措施:
(一)结合口诀对电化学题型进行解答;
(二)对溶液pH变化情况进行多方做题分析训练后适时引导并进行小结;
(三)根据离子类型判断介质中离子迁移方向;
(四)结合化学中的守恒思想做电化学题型;
(五)结合氧化还原反应原理解答此类题目;
(六)重点训练学生正确书写电极反应式。
电化学相关题型几乎每年都会在高考题中出现,而学生解答这类题目存在很大困惑。关于电化学题型解题思路与方法的分享有助于提高学生答题正确率。
参考文献:
[1]杨玲. 电化学在2019年高考中的考查[J]. 中学化学, 2020, 000(002):42-44.
[2]蒋红年. 电极反应式书写混乱原因及对策[J]. 化学教育(中英文), 2014, 35(5): 73-75
[3]张秀红. 有关可充电电池的解题方法[J]. 中学生数理化(教与学), 2015(12).
[4]苟坤德. 挖掘反应原理,提升解题技巧——以锂电池、燃料电池复习为例[J]. 高中数理化, 2018, 000(007):60-62
