白内障是一种因眼睛晶状体蛋白质变性改变而引发的视觉障碍性病症,病发后可导致患者出现视力逐步降低,视物模糊,对比敏感度下降等一系列视觉障碍,对其视物能力存在严重影响[1]。现阶段临床针对白内障的治疗用药主要包含谷胱甘肽、法可林、吡诺克辛等,但单纯药物在白内障治疗中疗效并不确切,往往只能延缓疾病进展。临床针对白内障的治疗手术方案较多,主要包含PE(超声乳化白内障吸除术,英文全称:Phacoemulsification)、白内障囊外摘除术、IOL(人工晶状体植入术,英文全称:Intraocularens)等,其中以PE+IOL为当前临床应用最为广泛的一种白内障治疗术式。该术式具有良好效果,可有效改善患者视力,满足其视觉改善需求;但其也存在术后AC(前房,英文全称:Anterior chamber)渗出风险,影响视力恢复效果[2]。现阶段临床针对AC渗出发生机制并不明确,但现有研究显示手术方式、手术时间、术中能量、器械过度使用、病患自身伴有眼部慢性炎症、晶状体混浊密度及部位等均可能引发术后AC渗出。对此,本次研究回顾性选取本院2020.1.1-12.31期间行PE+IOL治疗的白内障病例300例为研究对象,观察其术后AC渗出发生率,并分析影响PE+IOL术后AC渗出的相关因素,旨在强化防治,保障手术效果与安全性。内容如下。
1.资料与方法
1.1 一般资料
回顾性选取本院2020.1.1-12.31期间行PE+IOL治疗的白内障病例300例为研究对象,将其按照术后是否发生AC渗出进行分组,发生AC渗出者纳入研究组,未发生AC渗出者纳入参照组。研究经医学伦理委员会审核通过。
纳入标准:①符合《现代白内障治疗》[3]中与白内障相关的诊断标准;②在眼科裂隙灯检测下明确诊断;③临床资料完整;④均为单眼患病。
排除标准:①先天性或外伤性白内障;②既往有PE、IOL治疗史;③凝血障碍;④合并其他眼部疾病;⑤严重延伸功能不全;⑥伴认知障碍或沟通障碍。
1.2 方法
1.2.1 治疗方法
均行PE+IOL治疗,常规消毒铺巾,局麻后,角膜侧切口在2点钟方向作,长度在1 mm左右;透明角膜切口在10:30方向作,长度在3 mm左右,连续环形撕囊,水分离充分。以超声乳化仪(YD 10;苏州六六视觉)将晶状体吸出,植入人工晶体,水密闭合角膜缘切口,术毕。
1.2.2 统计PE+IOL术后AC渗出发生率
统计术后AC渗出发生病例数,计算AC渗出发生率。[AC渗出发生率=(发生AC渗出病例数÷总例数)×100%]。
1.2.3 相关因素分析
搜集整理相关研究资料,初步选择可能影响AC渗出的相关因素,采集病例资料,通过单因素、多因素Logistic分析,确定独立影响因素。具体过程如下:①相关因素选择:通过知网、万方、Google学术、SCI等搜索引擎查找文献资料,结合临床实际,初步确定可能与PE+IOL术后AC渗出发生的相关因素。最终将性别、年龄、高血压病史、吸烟/酗酒史、术前角膜内皮细胞计数、术前眼内压、青光眼、术中后囊膜破裂、高度近视、晶状体核分级、合并葡萄膜炎、术中瞳孔直径等资料纳入研究。②单因素分析:对比各因素不同分组患者术后AC渗出发生情况,初步确定可能影响术后AC渗出发生的影响因素。③多因素Logistic回归分析:将单因素对比存在差异项目纳入多因素Logistic回归分析中,赋值并建立回归分析方程,确定独立影响因素。
1.3 统计学方法
以SPSS 25.0软件统计数据。(![]() )、%分别表示计量、计数数据,t、χ2检验;独立影响因素采用Logistic回归分析,P<0.05时存在统计差异。
)、%分别表示计量、计数数据,t、χ2检验;独立影响因素采用Logistic回归分析,P<0.05时存在统计差异。
2.结果
2.1 PE+IOL术后AC渗出发生率
本次研究中20例患者发生AC渗出,发生率6.67%(20/300)。
2.2单因素分析
将20例发生AC渗出的患者纳入研究组;未发生AC渗出的280例为参照组。经单因素分析显示:眼科疾病(包含高度近视、青光眼、合并葡萄膜炎)、术前眼内压、术中后囊膜破裂、晶状体核分级、术中瞳孔直径等资料对比有统计差异(P<0.05)。见表1。
表1单因素分析

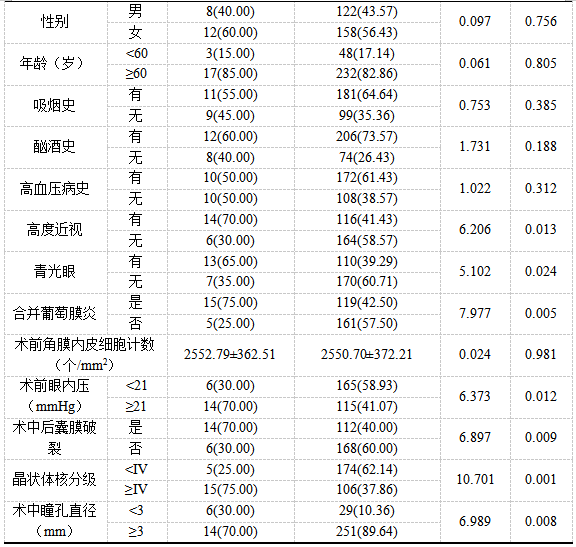
2.3多因素分析
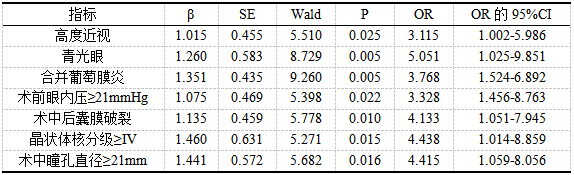
以“PE+IOL术后AC渗出”为因变量,以“2.2”中对比P<0.05的相关指标作为自变量,对相关指标进行赋值(具体如表2),展开多因素Logistic回归分析。研究显示:眼科疾病(包含高度近视、青光眼、合并葡萄膜炎)、术前眼内压(≥21mmHg)、术中后囊膜破裂、术中瞳孔直径(≥21mm)、晶状体核分级(≥Ⅳ)均为PE+IOL术后AC渗出发生的独立相关因素(均P<0.05)。详见表3。
表2赋值表
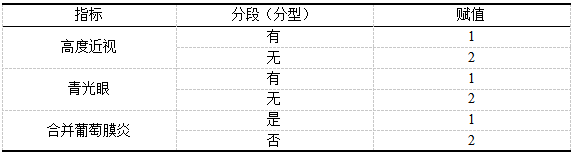
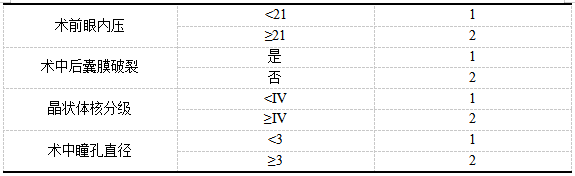
表3多因素Logistic回归分析
 3.讨论
3.讨论
白内障为临床高发眼科病症,其主要是由于中毒、遗传、外伤、代谢异常、免疫异常、局部营养障碍、辐射等因素引发的晶状体代谢紊乱,进而促使晶状体蛋白质变性混浊所致的眼科疾病[4]。PE+IOL在白内障治疗中具有疗效确切、创伤小、术后视力恢复良好等优势,为首选的白内障治疗方案;但PE+IOL术后眼球易发生无菌性炎症反应,导致AC渗出,促使患者术后出现视力减弱、结膜出血等症状,不利于预后恢复[5]。因而科学分析影响PE+IOL术后AC渗出的相关危险因素十分必要。
本次研究显示,300例患者中,PE+IOL术后AC渗出发生率为6.67%(20/300)。经多因素分析,眼科疾病(包含高度近视、青光眼、合并葡萄膜炎)、术前眼内压(≥21mmHg)、术中后囊膜破裂、晶状体核分级(≥Ⅳ)、术中瞳孔直径(≥21mm)等均为导致PE+IOL术后AC渗出发生的独立相关因素(均P<0.05)。分析原因可见,葡萄膜炎是由于手术刺激、长期炎症反应导致术后炎症控制难度增加,一旦处理不当则会导致前房炎症反复发作,并造成继发性青光眼,严重影响预后。因而可强化术前葡萄膜炎控制,并在术前评估是否处于炎症活动期,结合实际病情采取糖皮质激素类药物进行炎症控制。术前眼内压水平超过21mmHg情况下,患者血- 眼屏障功能、眼内外环境稳定性均相对较差,故PE+IOL术后易引发AC渗出;对此需在术前严格监测眼内压,针对高眼压病例需控制眼压后再行手术[6]。PE+IOL术中发生晶状体后囊膜破裂后,由于手术难度较高,易发生虹膜损失,从而引发AC渗出;对此,可在术前对晶状体后囊膜破裂风险进行评估,并严格制定针对性手术方案。青光眼白内障病例术前多需使用前列腺素类药物治疗,其可导致血- 眼屏障被破坏,增加PE+IOL术后AC渗出风险;对此,需严格核对患者术前用药史,针对近期有相关药物使用经历者延期手术。伴高度近视的白内障病例则多伴有严重的玻璃体液化,PE+IOL术中眼压稳定性相对差,也会增加手术难度,导致AC渗出风险增加,故需及时予以药物预防。晶状体核分级≥Ⅳ级病例手术治疗期间,对术中能量则有较大需求,术后恢复相对缓慢,故易引发AC渗出;故可适当延长术后观察时间,结合患者恢复情况予以相应干预,防范AC渗出。
综上,目前临床PE+IOL术后AC渗出发生风险仍相对较高,其中患者自身合并眼科疾病、术前眼内压高、术中后囊膜破裂、晶状体核分级≥Ⅳ级等均为AC渗出发生的独立危险因素,故在临床治疗期间可结合相关高危因素加以防治,科学降低术后AC渗出发生风险。
