中图分类号: O629.32
黄颜木素(Fustin,FT)又称二氢漆黄素(见图1),是一种天然双氢黄酮醇,主要来源于漆树科植物,存在于红花漆树(Rhus rhodanthema)、野漆树(Rhus succedanea L.)、红漆树(Rhus continus L.)和皂荚[1-3]中。其具有保护血管、抑制过氧化脂质的形成、抗癌[4]、抗炎[5]、抗氧化、抗肝纤维化、保护神经和防治心血管等生物活性。研究显示,黄颜木素对食管癌(EC109)、肝癌(HepG2)和肺癌(A549)均有较强的细胞毒活性,其细胞毒性与浓度有关。另外,黄颜木素可以显著抑制激活的永生型大鼠肝储脂细胞(HSC-T6细胞)的增殖,并减少转化生长因子β1(TGF β1)诱导的细胞内胶原合成,但黄颜木素水溶性差的特点,限制了黄颜木素在药物制剂方面的应用,因此,寻找一种高溶解度低毒性的药物载体显得尤为重要。
环糊精(Cyclodextrin,CD)合成简单、价格低廉,具有特殊的亲水外表和不同大小疏水空腔,是一种常见高浓度低毒的超分子药物载体。环糊精的空腔通过非共价键作用力如氢键、范德华力等,与天然药物分子形成主客体包合物,从而改善天然药物的理化性质,改善天然药物在药物制剂方面的应用。环糊精衍生物2-羟丙基β-环糊精(HP-β-CD)在水中的溶解度优于传统的CD,本课题组前期研究了漆黄素与β-环糊精衍生物、虫草素与HP-β-CD的主客体包合物,研究表明,漆黄素和虫草素与环糊精形成主客体包合物,其稳定性和溶解度均得到明显提高。基于此,高浓度低毒的环糊精作为天然药物载体的研究具有一定意义。
本文选用HP-β-CD作为药物载体,FT作为客体分子。采用饱和水溶液法制备FT/HP-β-CD包合物,通过核磁共振波谱法(1H-NMR、2D-NMR)、分子对接模拟、紫外-可见吸收光谱法(UV-Vis)、傅里叶变换红外光谱法(FT-IR)、扫描电镜(SEM)对包合物进行表征,进一步探究了其性能。结果显示,FT与HP-β-CD以1:1形成络合,为天然药物FT的应用研究提供实验依据。
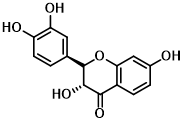
图1 FT的结构
1 实验部分
1.1 仪器与试剂
美国安捷伦公司紫外-可见分光光度计(Aglient 8453);瑞士 Bruker 公司核磁共振仪(Avance DRX 500);瑞士Bruker公司X-射线粉末衍射仪(Bruker D8 Advance A25X);美国Thermo Fisher Scientific公司傅里叶红外光谱仪(NICOLET iS10);美国 FEI 公司扫描电镜(Quanta200);上海天平仪器厂电子分析天平(FA1004);上海一恒科学有限公司真空干燥箱(DZF)。
FT(C15H12O6,ω>98%)购于宝鸡市辰光生物科技有限公司;2-羟丙基β-环糊精(HP-β-CD,C42H70O35)购于德国J&K SCientific 公司;实验中所有试剂均为分析纯,水均为纯净水。
1.2 实验方法
1.2.1 包合物的制备
按照摩尔比为1:1准确称取FT和HP-β-CD置于50 ml圆底烧瓶中,加入适量甲醇与水(VCH3OH:VH2O=1:4)混合溶剂,使其充分溶解,室温下避光搅拌反应4天,采用0.45 μm微孔过滤膜过滤,旋干,加适量纯净水除去不溶物,再过滤,真空干燥24小时,得到橙黄色包合物FT/HP-β-CD。
1.2.2 FT标准曲线的测定
配制储备液:利用甲醇溶液配制5 mmol/L的FT储备液。配制对照品:准确量取2、4、6、8、10、12、14、16、18、20、22、24 μL FT储备液,用混合溶剂(VCH3OH:VH2O=1:1)稀释,得到含FT 0.0033、0.0067、0.0100、0.0133、0.0166、0.0199、0.0232、0.0265、0.0298、0.0331、0.0364、0.0397 mmol/L的系列对照品溶液。测定最大吸收波长280 nm处FT溶液的吸光度。绘制标准曲线:FT溶液的浓度C为横坐标,吸光度A为纵坐标,其标准曲线为:A=26.119C-0.0907,R2=0.9993,结果表明,FT在0.0034~0.0397 mmol/L的范围内呈良好的线性关系。
1.2.3 Job՛s曲线
采用等摩尔连续变化法测定FT与HP-β-CD的包合计量比。用甲醇溶液分别配制5 mmol/L的FT和HP-β-CD母液,分别稀释母液为0.001 mmol/L,维持体系总浓度为1×10-4 mol/L,使得FT与HP-β-CD的摩尔比在0~1范围内变化,配制系列浓度梯度的混合溶液,测定最大吸收波长280 nm处的吸光度。
1.2.4 紫外-可见吸收光谱法(UV-Vis)
通过UV-Vis法探究FT与HP-β-CD间的主客体络合行为,用甲醇溶液配制5 mmol/L的FT和0.24 mol/LHP-β-CD母液,保持FT的浓度为1.6667×10-5 mol/L,按照等浓度梯度依次加入0-18 μL的HP-β-CD溶液,测定其紫外吸收光谱。
1.2.5 分子对接模拟
采用分子对接模拟计算FT与HP-β-CD包合模式。利用Gaussian Wiew构建FT的初始结构,用B3LYP/6-31G(d)对FT的结构进行优化至几何平衡;HP-β-CD的结构来源于剑桥晶体数据库,在无任何限制因素条件下采用MOPAC2016软件包完成进行优化。HP-β-CD设置为刚性受体,FT设置为分子柔性扭转配体,利用遗传算法,设置最大评估数2.5×106,执行1000次构象搜索,最后通过聚类分析得到一系列包合模式。采用AutoDock 4.2程序完成分子对接及计算。
2 结果与讨论
2.1 Job՛s曲线
按1.2.3的方法测定,以FT的摩尔分数为横坐标,FT与HP-β-CD的吸光度之差与FT的摩尔分数乘积为纵坐标绘制Job՛s曲线,如图2所示。结果显示,当摩尔分数为0.5时,溶液的吸光度之差与FT的摩尔分数乘积达到最大。由此可推测,FT/HP-β-CD的化学计量比为1:1。
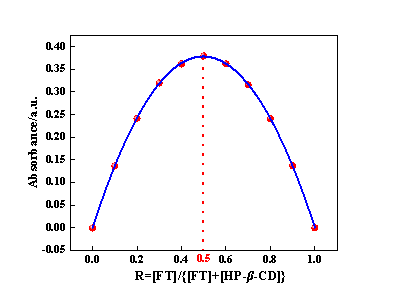
图2 FT与HP-β-CD的Job՛s曲线
2.2 紫外-可见光谱滴定(UV-Vis)实验
按1.2.4的方法测定紫外吸收光谱,探究FT与HP-β-CD间的主客体络合行为,如图3所示。由测试结果可知,随着HP-β-CD溶液的逐渐增加,混合溶液的吸光度也逐渐增强,说明FT与HP-β-CD之间存在着较强的主-客相互作用。根据滴定过程中吸光度的变化,采用BenesiHildebrand曲线法求解得FT与HP-β-CD的络合常数为1.6082×104 L/mol。
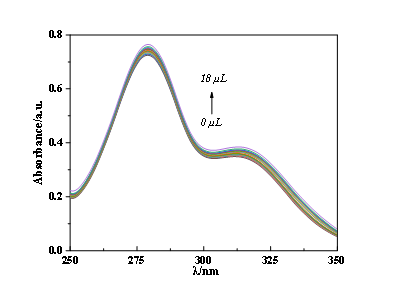
图3 FT与HP-β-CD的紫外-吸收可见光谱图
2.3 红外光谱分析
采用傅里叶变换红外光谱仪测试FT、HP-β-CD和FT/HP-β-CD的红外光谱,样品与溴化钾按照1:100的质量比进行研磨压片。
FT、HP-β-CD和FT/HP-β-CD红外光谱如图4所示,FT(见图4 a)在3440 cm-1处是芳环上-OH的伸缩振动峰,在3210 cm-1处是芳环上-H的弯曲振动吸收峰,在1670 cm-1处为H-C-H的弯曲振动吸收峰,在1533 cm-1、1470 cm-1处是苯环及双键中C-H弯曲振动峰,在850 cm-1处是不饱和C-H弯曲振动峰。HP-β-CD(见图4 c)在3440 cm-1处是-OH的伸缩振动峰,在2928 cm-1处是-CH和-CH2弯曲振动峰。FT与HP-β-CD形成包合物之后(见图4 b),由于受到HP-β-CD的影响,谱图上并没有完全显示出来,但是在1670cm-1处为吸收峰明显蓝移,在2928 cm-1、1533 cm-1、1547 cm-1、863 cm-1处的特征峰比HP-β-CD特征峰明显减弱,说明FT与HP-β-CD包合成功。
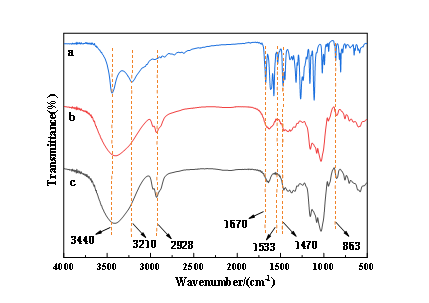
图4 FT(a)、FT/HP-β-CD包合物(b)、HP-β-CD(c)的FT-IR图
2.4 电镜分析
采用扫描电子显微镜测试FT、HP-β-CD和FT/HP-β-CD,样品均匀分布在金属样品台上,真空喷金处理,测试样品表面形态,通过对比包合前后物质的形态变化,初步判断包合物的形成。
FT、HP-β-CD和FT/HP-β-CD的电镜图如图5所示,FT的形态为长短不一的木条状,形似一堆整齐堆放的木条形(见图5 a);HP-β-CD的形态为含有空腔的圆球状结构(见图5 c);FT/HP-β-CD的形态为表面平整光滑的块状结构(见图5 b),FT的木条状和FT/HP-β-CD的空腔结构明显消失,包合后结构出现新的形态,表明FT/HP-β-CD包合成功。

图5 FT(a)、FT/HP-β-CD(b)包合物及HP-β-CD(c)的SEM图
2.5 核磁共振波谱分析
核磁共振是研究主客体之间包合物形成最有效的方式。采用核磁共振波谱仪分别测试FT、HP-β-CD和FT/HP-β-CD的1H NMR和2D NMR,FT溶于DMSO-d6,HP-β-CD和FT/HP-β-CD溶于99.80%的D2O中进行测试,四甲基硅烷(TMS)为氘代溶剂的内标。
主客体之间形成包合物之后,由于客体分子络合进入主体分子空腔内,导致主体分子质子发生化学位移,因此,采用1H NMR表征主体分子在包合前后质子化学位移的变化,从而推测包合物的形成。HP-β-CD和FT/HP-β-CD在D2O中的1H NMR如图5所示,FT/HP-β-CD的1H NMR中同时含有FT和HP-β-CD的特征质子峰,在δ 7.33 ~7.66 ppm范围内出现了FT的H12、H15、H16的质子峰,在δ 3.81 ppm出现了FT的H18的质子峰。

图 5 HP-β-CD与FT/HP-β-CD包合物的核磁共振氢谱(1H NMR)
FT与HP-β-CD包合后,HP-β-CD大部分质子的化学位移均发生一定的变化,HP-β-CD的质子化学位移如表1所示,其中H1、H2、H3质子移动了0.01 ppm;H5质子移动了0.03 ppm。将所有质子的化学位移进行对比分析,化学位移值变化最大是H5质子,推断FT从小口端H5进入HP-β-CD空腔。

表1 HP-β-CD和包合物的1H NMR化学位移值(δ)化学位移 δ (ppm)
FT/HP-β-CD的2D NMR如图6所示,FT的H18与HP-β-CD的H5存在NOE相关,推断FT/HP-β-CD包合物制备成功,结合图5的1H NMR数据及其HP-β-CD质子位移情况,结果显示,可推测FT是从HP-β-CD的H5小口端进去空腔内部形成包合物。

图6 FT/HP-β-CD的 2D NOESY、可能包合模式、关键NOE相关谱图
2.6 分子对接模拟
为了推测FT/HP-β-CD包合模式,按上文1.2.5中的方法进行聚类分析得到两种结合能最低的结合模型,如图7所示,模型结构中存在4个分子间氢键,键长分别为0.17、0.18、0.19、0.24 nm,均为O-H…O型氢键。这些分子间的氢键均小于0.30 nm,结果显示,FT与HP-β-CD主要以O-H…O型氢键作用形成包合物。该结果与1H NMR、2D NMR的结果一致。

图7 FT与HP-β-CD分子对接最稳定的包合模式
3 结语
本文首先利用饱和水溶液法制备FT/HP-β-CD包合物。然后利用傅里叶红外光谱(FT-IR)和电子扫描电镜(SEM)对FT/HP-β-CD进行表征,采用Job՛s曲线分析FT与HP-β-CD之间包合比,结果表明,主客体包合物以包合比为1:1制备成功。利用核磁共振(1H-NMR、2D-NMR)对FT/HP-β-CD的包合模式进行推测,结果显示,FT从HP-β-CD的H5小口端进行HP-β-CD空腔内,并且FT/HP-β-CD之间主要以氢键作用形成,为FT的后续应用提供实验理论基础。
参考文献
[1]陈虹霞,王成章. 漆树黄酮类化合物研究进展[J]. 天然产物研究发, 2013,25(12): 1752-1758.
[2]罗千洙,郑南澈,罗垠善. 漆树提取物的制备方法及包含该提取物的抗癌组合物[P]. 韩国:CN98101629.4, 2006-12-13.
[3]陈海霞,肖顺汉. 皂角刺抗肿瘤作用有效成分研究进展[J]. 四川生理科学杂志, 2010,32(01): 35-37.
[4]李文基,马骏,赵文秀. 皂角刺抗肿瘤药理作用及化学成分研究进展[J]. 甘肃中医药大学学报, 2020,37(06): 85-88.
[5]Li K K ,Shen S S ,Deng X , et al. Dihydrofisetin exerts its anti-inflammatory effects associated with suppressing ERK/p38 MAPK and Heme Oxygenase-1 activation in lipopolysaccharide-stimulated RAW 264.7 macrophages and carrageenan-induced mice paw edema[J]. International Immunopharmacology, 2018, 54366-374.
基金项目:国家自然科学基金项目(No. 21762051);云南省高校有机功能分子及材料科技创新团队项目和云南省教育厅科学研究基金项目(No. 2023J2243)
