含铂类药物化疗是目前恶性肿瘤治疗的重要方式,对于铂类抗肿瘤药物的研究兴起于1967年,美国密执安州立大学教授Roserlberg首次发现并提出顺铂具有抗肿瘤活性,从此铂类药物成为抗肿瘤药物治疗的首选[1-3]。据数据统计显示,我国70%-80%的化疗方案均有铂类药物参与配伍[4],但化疗后不良反应尤为明显,有研究表明,采用含铂类药物化疗的恶性肿瘤患者,未经任何人工预防控制,其恶心、呕吐率可达90%[5],对患者治疗效果存在不利影响。故此,以防治胃肠道不适为基础的治疗尤为重要,本次研究将帕洛诺司琼作为预防胃肠道不适的主要药物,研究其药物疗效及安全性,研究结果如下。
1 资料与方法
1.1临床资料
选取我院2017年3月至2021年5月期间收治的40例使用含铂肿瘤患者为研究对象。纳入标准:①经病理学或组织病理学诊断为恶性肿瘤者;②均接受标准计量含铂类为主的联合化疗,以顺铂、奥沙利铂为主;③所有患者预计生存时长均≥3个月,且一般健康状态评分(PS评分)≤2分;④一般资料完整,签署知情同意书。排除标准:①合并高颅压、慢性喉炎等其他可引发恶心、呕吐症状疾病者;②精神异常,认知障碍者;③合并其他躯体重大疾病者;④依从性较差、病情突然恶化、药物过敏者;⑤处于妊娠期、哺乳期者。所有患者依据奇偶数分组法分为两组,对照组和观察组各20例。观察组为偶数:男13例,女7例,年龄51-79岁,平均年龄(65.70±9.87)岁。对照组为奇数:男18例,女2例,年龄45-74岁,平均年龄(64.05±9.71)岁。两组基线资料对比无统计学差异(P>0.05)。
1.2治疗方法
对照组:给予格拉司琼治疗,于化疗前30min静脉滴注格拉司琼3mg,每日一次。
观察组:给予帕洛诺司琼治疗,于化疗前30min静脉滴注0.25mg帕洛诺司琼与100mL生理盐水混合溶液,每日给药一次。
当患者治疗后呕吐次数≥2次时,需进行人工干预给予对症药物解救,若患者呕吐剧烈择需根据患者实际情况进行追加、升级药量。化疗期间定时定期复查患者血常规、肝肾功能、电解质等基本情况。
1.3观察指标
(1)急性呕吐、延迟性呕吐控制率对比;急性呕吐为化疗24小时内发生恶心呕吐,5-6小时达到高峰,持续18个小时以上后转为慢性呕吐或呕吐停止。延迟性呕吐为化疗24小时-48小时以后出现的恶心呕吐情况,部分患者可持续一周。以完全控制、部分控制、轻微控制、无效控制作为呕吐控制率界定标准[6],完全控制:无恶心、呕吐症状;部分控制:每日呕吐次数≤2次,恶心次数≤12次;轻微控制:3次<每日呕吐次数<5次,5次<恶心次数<12次;无效控制:每日呕吐次数>5次,恶心次数>12次,或患者存在电解质紊乱,脱水等情况均视为无效控制。控制率=完全控制率+部分控制率
(2)营养状态对比:营养状态以白蛋白(ALB)水平与营养评定量表(PG-SGA)进行评定。PG-SGA为A表明营养状态良好,B+C则为营养状态较差,即认定营养不良。
(3)呕吐程度、生活质量评分对比:对两组患者治疗前后的恶心呕吐程度进行分级评定[7],0:无恶心、呕吐症状;I:出现恶心、呕吐症状,但不影响正常进餐与生活;II:轻度呕吐,在可控范围内;III:相对严重的呕吐,采取治疗后可控。生活质量以SF-36进行评价,总分100分,分数与生活质量呈正相关。
(4)不良反应对比:观察比较化疗期间两组患者不良反应发生情况,包括白细胞减少、肝肾毒性、头痛、便秘等。
1.4统计学分析
将SPSS20.0处理软件作为处理此次研究中数据的主要方法,对于此次研究中的计量资料用均数±标准差表示,采用t检验,计数资料用(%)表示,用χ2检验,检验结果P<0.05,提示差异具有统计学意义。
2 结果
2.1两组急性呕吐、延迟性呕吐控制率对比
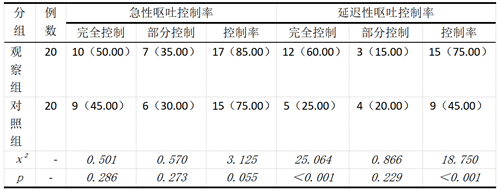
两组患者急性呕吐控制率无显著差异;观察组延迟性呕吐控制率明显高于对照组,差异具有统计学意义(P<0.05)。见表1。
表1:两组急性呕吐、延迟性呕吐控制率对比[n(%)]
2.2两组营养状态对比
观察组患者ALB水平显著高于对照组,且观察组PG-SGA评级为A的人数显著多于对照组(P<0.05)。见表2。

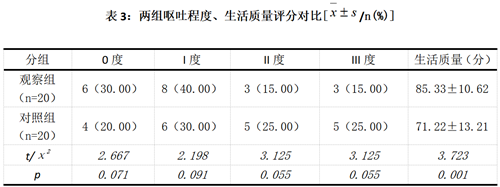
2.3两组呕吐程度、生活质量评分对比
观察组0度、I度比例显著高于对照组;II度、III度比例显著低于对照组,生活质量评分显著高于对照组,数据对比差异显著,具有统计学意义(P<0.05)。
2.4两组患者不良反应对比
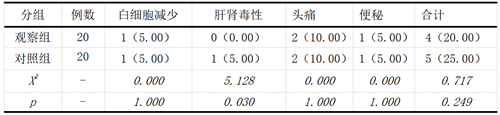
两组患者不良反应发生率比较,差异无统计学意义(P>0.05)。
表4:两组不良反应对比[n(%)]
3讨论
恶性肿瘤患者化疗是常规治疗方式,但30%-45%的肿瘤患者在化疗期间均会出现恶心、呕吐症状,需要医师进行止吐干预,称之为化疗性恶心呕吐(CINV)。以铂类药物为基础的联合化疗方式是恶性肿瘤治疗标准方案,如未经预防处理,90%的患者可出现CINV,对患者后期化疗效果产生负面影响。2003年7月,帕洛诺司琼(palonosetron)因其独特的长效性与高选择性被美国食品药品监督管理局承认为第一个可用于中度致呕性化疗药物引发CINV症状的预防药物,目前帕洛诺司琼已在40多个国家上市销售,成为治疗急性CINV的5-HT3受体拮抗药物[8-10]。
本次研究选取40例恶性肿瘤患者分别给予帕洛诺司琼、格拉司琼,结果显示采用帕洛诺司琼的观察组患者急性呕吐控制率与对照组相仿,延迟性呕吐控制率显著优于对照组,表明洛诺司琼可用于预防化疗诱发的呕吐。此项数据由于本组样本数量较小,有待进一步研究观察。同时观察组患者ALB水平显著高于对照组,PG-SGA评级为A的人数显著多于对照组,0度、I度比例显著高于对照组;II度、III度比例显著低于对照组,生活质量评分显著高于对照组,表明观察组患者与对照组相比,机体营养状态更佳,呕吐严重程度较低,日常生活质量更优。帕洛诺司琼的高选择性、高亲和力使其与5-HT3受体的结合度是同类药物的30倍之多,能够达到高效正协同作用,其作用于机体中枢神经外周神经元突触前5-HT3受体,在阻断受体兴奋的同时也可阻断胃肠道自主神经末梢的信号传递,达到降低恶心呕吐发生率的效果[11-13]。且帕洛诺司琼经静脉注射入人体后,其清除半衰期时长为40小时,与血浆蛋白的结合率为62%[14-15],能够在短效内达到药物峰值,快速发挥药效,缓解患者呕吐症状。除此之外,本次研究中观察组患者不良反应与对照组无显著差距,表明帕洛诺司琼药物安全性较高,不会对患者造成严重影响。帕洛诺司琼在人体中通过肾脏代谢,当静脉注射药物144小时后,约83%的药物可通过肾脏排泄出体外,表明帕洛诺司琼与临床药物相互作用可能性较低,其安全性进一步提升。
综合所述,帕洛诺司琼在恶性肿瘤患者含铂类药物化疗预防胃肠道不适的效果显著,疗效确切,且不良反应在预控范围内,安全性较高,在临床中具有较好应用前景。
参考文献
[1] 胡倩倩,王振辉,牛超,等. 铂类抗肿瘤药物耐药机制研究进展[J]. 药学进展,2017,41(10):769-774.
[2] 祝天慧,李裕鑫,游松. 铂类抗肿瘤药物的研究进展[J]. 沈阳药科大学学报,2016,33(6):512-518. DOI:10.14066/j.cnki.cn21-1349/r.2016.06.016.
[3] 杨谨成,贾贝,费小非,等. 我国各地医保目录中抗肿瘤药物类基本药物的收载情况分析[J]. 中国药房,2015(30):4181-4184. DOI:10.6039/j.issn.1001-0408.2015.30.02.
[4] 谭书想. 常见铂类抗肿瘤药物耐药机制和不良反应的比较分析[J]. 中南药学,2015,13(5):517-520. DOI:10.7539/j.issn.1672-2981.2015.05.019.
[5] 牟倩倩,刘珊珊,汪秀云,等. 肺癌首次铂类化疗所致恶心呕吐现状及心理状况分析[J]. 重庆医学,2018,47(26):3445-3449. DOI:10.3969/j.issn.1671-8348.2018.26.021.
[6] 王玉璇,李峰,彭胜祖,等. 盐酸帕洛诺司琼减轻非小细胞肺癌术前含铂类新辅助化疗所致消化道反应的临床价值[J]. 中国药物与临床,2014,14(4):517-519. DOI:10.11655/zgywylc2014.04.051.
[7] 李小洁,杨红霞,王梅,等. 隔药灸联合昂丹司琼在预防铂类化疗药物致恶心呕吐的临床研究[J]. 实用癌症杂志,2020,35(5):863-866. DOI:10.3969/j.issn.1001-5930.2020.05.044.
[8] Wong EH, Clark R, Leung E, et al. The interaction of RS 25259-197, a potent and selective antagonist, with 5-HT3 receptors, in vitro. Br J Pharmacol, 1995, 114(4):851-859.
[9] 龙国贤,胡广原.国产帕洛诺司琼预防化疗所致不良反应的临床观察[J].中华医院感染学杂志,2010,(第13期).
[10] Grunberg SM, Koeller JM. Palonosetron: a unique 5-HT3-receptor antagonist for the prevention of chemotherapy-induced emesis. Expert Opin Pharmacother, 2003,4(12):2297-2303.
[11] 王海凤,王东凯. 5-HT3受体阻滞剂帕洛诺司琼[J]. 中国新药杂志,2006,15(10):833-835. DOI:10.3321/j.issn:1003-3734.2006.10.025.
[12] 徐睿,姜虹. 帕洛诺司琼用于预防术后恶心呕吐的研究进展[J]. 国际麻醉学与复苏杂志,2013,34(5):441-443,460. DOI:10.3760/cma.j.issn.1673-4378.2013.05.014.
[13] 罗霞, 彭六保, 谭重庆,等. 帕洛诺司琼:第2代5-羟色胺3受体拮抗药[J]. 中国新药与临床杂志, 2009, 28(9):649-653.
[14] Hunt TL, GallagherSC, Cullen MT JR, et al. Evaluation of safety and pharmacokinetics of consecutive multiple-day dosing of palonosetron in healthy subjects. J Clin Pharmacol, 2005, 45(5):589-596.
[15] 王鹏、易红、李雪、林勇. 帕洛诺司琼预防术后恶心呕吐的有效性与安全性的系统评价[J]. 中国医院用药评价与分析, 2020, v.20;No.197(11):91-95+99.
