Report on isolation and identification of Salmonella
in milk powder
YANG Liu-qing1, LI Yan-hua2
(1. 2.Jiangmen Provincial Institute of Food Inspection, Jiangmen 529000, China)
Abstract: [Objective] To analyze and summarize the process of isolation and identification of Salmonella in milk powder. [Methods] According to the project guidance of proficiency testing, qualitative testing was carried out according to the national safety standard of food microbiology test for Salmonella (gb4789.4-2016). The biochemical identification instrument used was ATB automatic microbial identification system. [Results] In this proficiency test, there were 2 samples, and a total of three strains were isolated. One sample detected Salmonella and Escherichia coli, and one sample detected Citrobacter freundii. [Conclusion] This proficiency testing project is satisfied with the consistency, detection ability and detection level of Salmonella in milk powder. Our laboratory has the technical ability to detect Salmonella in food.
Key words: Ability verification; Salmonella; Escherichia coli; Citrobacter ferrardi ? Citrobacter freundii
1 引言
沙门氏菌属(Salmonella)、枸橼酸杆菌属(Citrobacter)、埃希氏菌属(Escherichia)为生物学性状相似的革兰氏阴性杆菌,属肠杆菌科。本次能力验证的目标菌沙门氏菌有2600个不同的血清型[1],按照GB4789.4-2016《食品安全国家标准食品微生物学检验 沙门氏菌检验》,符合沙门氏菌属相关典型的生化特性以及血清学鉴定鉴定到属,报告25g(mL)样品中检出或未检出沙门氏菌。本次能力验证分离鉴定过程中,应用ATB全自动微生物鉴定析系统,鉴别出三个致病菌属,和能力验证技术报告分析相一致。
2 材料和方法
2.1试验材料
2.1.1待测样品
乳粉中沙门氏菌检测能力验证样品有2个,分别为黄色标签和白色标签。样品为乳白色块状固体物,安培瓶真空密闭包装。
2.1.2培养基及试剂
本次能力验证使用商品化粉末培养基:缓冲蛋白胨水(BPW)、四硫磺酸钠煌绿(TTB)增菌液和配套试剂,亚硒酸盐胱氨酸(SC)增菌液、木糖赖氨酸脱氧胆盐(XLD)琼脂、营养琼脂(NA)、 沙门氏菌显色培养基(SA)、亚硫酸铋琼脂(BS)、HE培养基,生化鉴定使用沙门氏菌生化鉴定盒(通用型、EasyID)均购自广东环凯微生物有限公司。沙门氏菌A-F“O”多价诊断血清、沙门氏菌属Vi因子诊断血清,购自宁波天润。一次性培养基ATB全自动微生物鉴定系统配套试剂条(ID32E)为生物梅里埃产品。
2.1.3 主要仪器
生物安全柜、培养箱、高压蒸汽灭菌锅、生物显微镜(蔡司)、ATB全自动微生物鉴定/药敏分析系统( 法国生物梅里埃公司)、移液器。
2.1.4 标准菌株
乳粉中沙门氏菌定性分析质控样品、鼠伤寒沙门氏菌ATCC14028、伤寒沙门氏菌CMCC(B)50071。
2.2检测方法[2]
2.2.1样品处理
按照作业指导书,无菌打开安培瓶,用60mL无菌稀释液水化,等同于60mL乳粉样品作为待测溶液。按照GB4789.4-2016《食品国家安全标准 食品微生物学检验 沙门氏菌检验》。同时做空白对照和阳性对照。
2.2.2增菌
(1)前增菌:每个样品各吸25mL至225mL缓冲蛋白胨水BPW增菌液中,混匀后36℃±1℃培养18h,每个样品做2个平行样进行检测。
(2)选择性增菌。
无菌移取1mL,转种于增菌液TTB内42℃±1℃培养24h;同时另取1mL,转种于增菌液SC内,36℃±1℃培养24h。
2.2.3 分离培养
每个增菌液分别接种XLD、BS、HE、沙门氏菌显色培养基,36℃±1℃培养24-48h;
增菌分离培养情况见表1
表1 增菌分离培养情况 2.2.4生化鉴定和血清凝集实验
2.2.4生化鉴定和血清凝集实验
分别用环凯的生化鉴定盒(通用型、EasyID)、梅里埃的ATB生化试剂条ID32E对可疑菌落进行生化鉴定鉴定。结果详见表2。生化鉴定结果显示,D样品中检测出伤寒沙门氏菌、大肠埃希氏菌,F样品检出费劳地柠檬酸杆菌,质控样品检出沙门氏菌、大肠埃希氏菌;血清凝集试验,D样品中的伤寒沙门氏菌多价血清凝集。生化鉴定情况表2
表2生化鉴定情况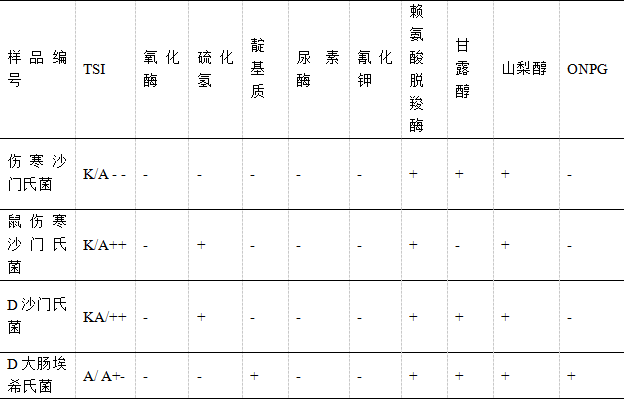
3结果与分析
3.1分离培养
本次分离培养过程中,F样品(费劳地柠檬酸杆菌)比D样品(沙门氏菌和大肠埃希氏菌)在TTB和SC增菌液混浊,容易让人误以为F样品才是阳性菌。
3.2判定
经生化鉴定和血清鉴定,D样品检出沙门氏菌,F样品为未?检出沙门氏菌。结论与能力验证预设一致,结果评价为满意。
4讨论
本次能力验证目标菌1个,干扰菌1个,阴性菌一个。在分离鉴定的过程中干扰菌大肠埃希氏菌干扰性不强,阴性菌费劳地柠檬酸杆菌迷惑性较强;
本次能力验证的分离出的沙门氏菌、大肠埃希氏菌、费劳地柠檬酸杆菌为具有典型性状的菌株,实验室可留作工作菌株使用;
本次能力验证对所使用的培养基作为一次有效的培养基验收,除了常用的生化鉴定试剂,新型的生化鉴定试剂盒(EasyID)操作便利、有效,可作为今后选用的生化鉴定试剂;
本次能力验证能经TSI、分离平板已经能有效辨别出阳性菌和阴性菌,但分离鉴定到具体菌属,应用设备ATB全自动微生物鉴定/药敏分析系统进行鉴别。
参考文献:
[1]周庭银,章强强,临床微生物学诊断与图解.第4版[M]. 上海科学技术出版社, 2017,9:315
[2]GB 4789.4-2016食品安全国家标准 食品微生物学检验 沙门氏菌检验










