盐酸特比萘芬片属于丙烯胺类抗真菌药物,该药物主要有三种类型分别为外用剂型和乳膏剂型合以及搽剂,主要作用为对皮肤真菌感染方面的治疗,在对该药物进行使用的过程中为了增加局部用药浓度并且对本院的制剂剂型进行拓展,基于此文章将会针对盐酸特比萘芬片的制备与质量控制方法进行详细的分析,如下文所示。
1仪器与试药
岛津LC-2010C型高效液相色谱仪(带工作站);Spheri RP-18柱(150 mm x 4.6 mm,5μm);DEL-TA320型pH计(METTLER TOLEDO);AS-3120型超声波发生仪;岛津UV-2450型分光光度仪;药物稳定性实验箱(重庆永生实验仪器厂)。盐酸特比萘.芬对照品(天津市药品检验所,纯度为99.7%);盐酸特比萘芬的有关物质对照品(齐鲁制药厂);盐酸特比萘芬凝胶(自制,规格20 g:0.2 g);卡波姆940(美国诺誉化工有限公司);甘油、三乙醇胺.乙醇等试剂均为分析纯,水为纯化水。
2处方及制备方法
2.1处方
盐酸特比萘芬10g,二甲亚砜10 mL,7 g卡波姆940,三乙醇胺14 g,丙二醇50 g,乙醇100 mL,10 g聚山梨酯-80,纯化水加至1 000 g。
2.2制备方法
首先是对卡波姆进行适量的称取,所称取的量为940,在称取的卡波姆中加入适量的纯化水对其进行浸泡最终达到完全溶胀的效果,该环节后在将三乙醇胺加入到其中进行中和,最后将中和后的液体中加入丙二醇、乙醇衱聚山梨酯-80,进行均匀搅拌;其次是对盐酸特比萘芬进行适量的称取,将二甲基亚砜加入到盐酸特比萘芬当中,对其进行均匀的搅拌并且在搅拌的过程中加入之前制备好的卡波姆混合液中,最后将纯化水加入其中并进行均匀搅拌。
3质量控制
3.1性状本品为乳白色均匀细腻的凝胶。
3.2鉴别
3.2.1紫外光谱
对本品进行适量的量取,在本品中加入乙醇并且将溶液的含量规定为每1毫升中含有20微克,采用照分光光度法对其含量进行测定,经过测定后可以了解到字283nm波长位置的吸收是最大的,而在258nm位置的吸收量是最小的,在274nm波长处会出现一处肩峰。
3.2.2高效液相色谱
本品含量测定项下记录的色谱图中,供试品主峰的保留时间应与对照品主峰的保留时间一致。
3.3检查
3.3.1pH值取
本品5g,置25ml.量瓶中,加适量乙醇,超声处理3)min,放至室温,用乙醇稀释至刻度,摇匀,滤过,精密量取续滤液5mL,置10mL.量瓶中,用水稀释至刻度,摇匀,依法测定(中国药典2000年版,二部附录VI H),pH值应为6.0)~8.0。
3.3.2有关物质取
本品适量(约相当于盐酸特比萘芬20mg),置100mL量瓶中,加乙醇80mL,超声振荡40min使盐酸特比萘芬溶解,放冷,用乙醇稀释至刻度,摇匀,滤过,精密量取续滤液适量,用流动相分别制成每1 mL中含10,0.05μg的溶液,作为供试品溶液和对照溶液,照含量测定项下的色谱条件,取对照溶液20μL注人液相色谱仪,调节检测灵敏度,使主成分峰高约为满量程的10%,再精密量取供试品溶液和对照溶液各20μL分别注人液相色谱仪,记录色谱图至主成分保留时间的3倍,供试品溶液如显杂质峰,其中单-杂质峰的峰面积不得大于对照溶液峰面积的1/2(0.25%);各杂质峰面积的和不得大于对照溶液的峰面积(0.5%)。
3.3.3其他应符合凝胶剂项下有关的各项规定(中.国药典2000年版二部附录I U)。
4试验方法的研究
4.1有关物质的试验方法
4.1.1方法研究
将5个有关物质杂质对照品加入盐酸特比蔡芬对照品中,制备适宜浓度的混合对照品(502-82,206-89,533-93,503-82,532-86)溶液,按拟定的色谱条件进行分析,杂质与主峰间分离度均符合要求,主峰出峰位置在503-82与532-86之间,典型色谱图如图1所示,各混合对照品的色谱图如图1所示。样品中杂质实际含量较少,采用不加校止因子的自身对照法计算有关物质的含量,限度规定为:单一杂质不得过0.25%;总杂质不得过0.5%。
4.1.23批样品有关物质的测定结果照“3.3.2"测定,结果各单个杂质(0.01%~0.21%)和总杂质(0.27%~0.37%)的量均符合拟定标准。
4.2含量测定的试验方法
4.2.1方法研究
为了使分析方法适用于本制剂及有关物质的分离。
(1)干扰试验精密称取凝胶样品约2g,置100mL量瓶中,加乙醇80mL,超声振荡40min,使盐酸特比蔡芬溶解,放冷,用乙醇稀释至刻度,摇匀,滤过,精密量取续滤液适量,用流动相制成每1mL中含2μg的溶液,按上述色谱条件进行测定;按处方制备不.含主药的空白凝胶基质.依法进行测定,结果表明,空白凝胶基质不影响主药测定。
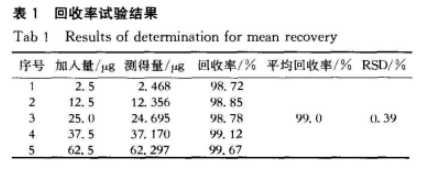
(2)回收率试验取空白凝胶基质约25 mg,精密称定,置100mL量瓶中,加适量乙醇,超声处理使澄清,放冷,用乙醇稀释至刻度,摇匀,滤过,分别精密量取续滤液15mL,置5个25mL量瓶中;分别精密量取“线性关系考察"项中5种不同浓度的溶液各1mL,置上述5个25mL量瓶中,用流动相B稀释至刻度,按拟定的色谱条件测定。将测得的峰面积代人线性方程中,求得盐酸特比茶芬的浓度,进而求得回收率。回收率结果见表1。
 5讨论
5讨论
对比流动相需氢氧化四乙基胺离子和磷酸盐缓冲液,这两种流动相中一种需要对特殊试剂进行使用,另一种则需要对盐类进行使用,不过这种盐类会对色谱柱造成一些危害。也正是因为这种情况,在本文的研究过程中使用的流动相为甲醇-水-三乙胺系统,该系统具有较为温和的特点。考虑到盐酸特比萘芬为萘胺类物质呈现的是碱性,在其中加入三乙胺后可以将碱性进行融合同时三乙胺可以和残余的硅醇基之间产生相互作用,有效的将实验中的拖尾现象进行消除或者是减弱。因为在分析组中包含了多种分数目并且各种分数目之间的差异性较大,因此在实验中采用的是梯度洗脱方法,通过这种方法可以有效的缩短分析时间,其分离度也会得到提高。卡波姆是由丙烯酸与丙烯基蔗糖互相之间进行联合后形成的一种聚合物,该聚合物的特点为具有较强的吸湿性,不会对皮肤和粘膜带来刺激,具有良好的皮肤耦合性,当涂在皮肤上后会形成透明薄膜,该薄膜经过水冲洗后则可去除,另外涂抹后所形成的薄膜具有良好的耐寒和耐热性。由此可见将卡波姆用作基质制备凝胶剂的优点为没有油腻感、释药快、易药快且可以便于清晰。将该药物涂抹在皮肤表面后可以较强的附着在皮肤表面上,对药物的药效具有增强的作用。
参考文献
[1]郎伟君.一种盐酸特比萘芬片,其制备方法以及杂质与质量检测方法:,CN112156078A[P].2021.
[2]王学艳,寇欣,王雷.盐酸特比萘芬凝胶的制备与质量控制[J].中国医院药学杂志,2005,25(7):3.
[3]张锦.盐酸特比萘芬栓剂含量测定方法的研究[J].药物分析杂志,2008(10):1764-1766.










