恶性浆膜腔积液与肿瘤晚期转移或直接侵犯浆膜腔有关。细胞学检查因简便、快捷、安全、准确,被广泛应用于肿瘤的诊断。传统的细胞学检查在在肿瘤诊断中有一定的局限性,如样本不能长期保存、收集细胞数量不足、依赖病理医生诊断经验等。随着精准医学的不断发展,对细胞学诊断有了更高的要求。
EC CB可反复多次、多切面连续切片,结合免疫组织化学(Cimmunohistochemistry IHC)技术很好地降低了细胞学诊断的漏诊率及误诊率,提高了诊断的准确率,为患者预后及治疗提供更精准的方案。本文收集活检组织病理确诊为恶性肿瘤的病例40例,探讨EC CB免疫组化技术在肿瘤诊断中的临床应用价值。
1 材料与方法
1.1 材料 收集天水市第四人民医院病理科2021年5月-2022年11月确诊为恶性浆膜腔积液的40例患者的临床病理资料,其中男性28例,女性12例,男女比例2.3:1,男性平均年龄(46-80岁)61.8岁,女性平均年龄(48-77岁)66.2岁。所有患者均行EC CB免疫组化,并与活检组织病理诊断结果进行对比分析。浆膜腔积液标本采集均由本院临床医生穿刺取得30min内送至病理科。
1.2 方法
1.2.1 ①传统细胞学涂片:取适量浆膜腔积液放入10ml离心管中,离心机2000r/min,离心10min,弃上清液,棉签取适量底部沉淀均匀涂至载玻片上,适量95%乙醇固定,吉姆萨染色,封片,阅片。②细胞蜡块切片:细胞蜡块常规切片后与组织切片一起行HE染色,封片,阅片。
1.2.2 细胞蜡块的制作 取细胞学涂片后剩余浆膜腔积液全部批量放入50ml离心管中,离心机2000r/min,l离心10min,弃上清液(血性标本先加入3%醋酸乙醇10ml,震荡均匀,离心,去除血细胞干扰);向沉淀物中先加入10%中性福尔马林5ml,震荡,离心,弃上清液;后加入75%乙醇10ml,震荡,2000r/min,离心10min,弃上清液,再加入95%乙醇10ml,震荡,2000r/min,离心10min,弃上清液,底部沉淀镊取至滤纸上,包好,与常规组织一起行脱水处理,制成细胞蜡块。
1.2.3 免疫组化 用细胞蜡块制作3um 厚切片,免疫组化采用MaxVision法,具体操作步骤按试剂盒说明书进行染色。一抗选用PCK、TTF-1、NapsinA、P40、P63、Syn、CgA、CD56、CD45、CD3、CD20、D2-40、Vimentin、P16、Calretinin、WT-1、PAX-8、CK7、CK20、CDX-2、CAM5.2、CEA、Villin、Hepatocyte、P16、ER、PR、C-erbB-2、AFP、CD10、P53、Ki-67等。试剂购于福州迈新生物技术开发公司。
1.2.4 统计学方法
采用SPSS21.0对数据进行统计学分析。计数资料以率(%)表示,组间比较采用X2检验。分别计算敏感度、特异度、假阳性率、假阴性率和诊断符合率。
2 结果
2.1 免疫组化分型 40例浆膜腔积液细胞蜡块经免疫组化证实肺腺癌15例,肺鳞状细胞癌3例,肺小细胞癌1例,肝细胞癌1例,肝胆管细胞癌2例,胰腺导管腺癌2例,乳腺癌1例,宫颈鳞状细胞癌1例,胃肠腺癌7例,卵巢浆液性7例(表1)。
2.2 细胞学制片观察 恶性浆膜腔积液中以腺癌多见。细胞涂片:肿瘤细胞核大、畸形核,核膜增厚欠光滑,深染,核浆比失调,细胞黏附性较强,易凝集成团、块。细胞蜡块HE切片:肿瘤细胞量多,散在、成簇状分布,细胞结构清晰,高核浆比,染色质粗,部分核仁明显,可见腺腔等相对应的肿瘤组织学结构。
2.3 明确肿瘤来源及类型 细胞蜡块免疫组化染色(图5、6),着色清楚,定位准确,结合患者临床资料、细胞学特点及免疫组化结果,明确肿瘤来源及类型(表1),同时进行鉴别诊断。
2.4 脱落细胞学细胞蜡块(EC CB)免疫组化与活检组织免疫组化病理诊断结果比较
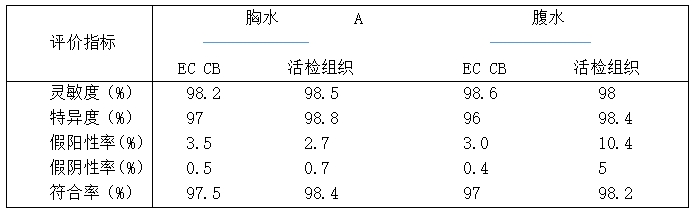
EC CB 联合IHC具有较高的病理诊断符合率,胸水为97.5%,腹水为97%;活检组织联合IHC诊断符合率胸水为98.4%,腹水为98.2%,x2=6.40,P=0.03(表2)。
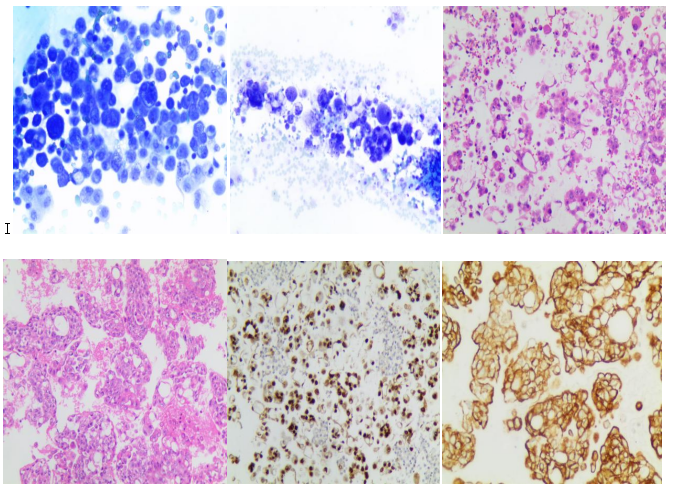
图1、2传统细胞学涂片:腺癌细胞核浆比高,巢团、片块状排列,分布不均匀,重叠,凝集成块,吉姆萨染色。图3、4 细胞蜡块切片:细胞量多,结构清晰,显示组织学结构,HE染色。图5:胸水肺腺癌:TTF-1阳性(MaxVision法)。图6:胸水卵巢浆液性癌:CK7阳性(MaxVision法)。
表1 浆膜腔积液脱落细胞蜡块免疫组化分型诊断结果(n=40例)
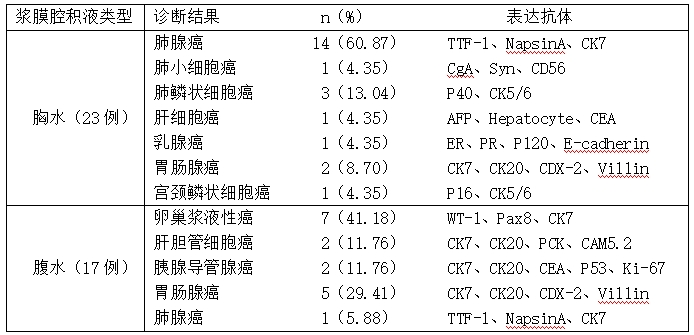
表2 EC CB结合IHC与活检组织IHC病理诊断比较
3 讨论
浆膜腔积液是大多数肿瘤患者晚期常见并发症之一,因部分原发病灶隐匿,等发现时已出现转移,患者往往以浆膜腔积液为首发症状收住入院。晚期患者已失去手术机会,需要的只是明确诊断,进行保守治疗。浆膜腔积液细胞蜡块免疫组化能很好的明确肿瘤来源及性质,并分类,对患者的治疗及预后具有重要意义。是一种值得推广的微创诊断方法。
细胞蜡块包埋技术在国内外许多医院已成为细胞学常规诊断技术。高水平的阅片离不开医师的诊断水平,浆膜腔积液中最常见的是腺癌,诊断中最大的挑战是间皮细胞、组织细胞与肿瘤细胞,特别是腺癌细胞的鉴别诊断。因免疫组化标志物种类繁多,其敏感性和特异性各异,要求诊断医师熟练掌握各种肿瘤细胞与其它细胞免疫标志物的表达特点,对浆膜腔积液做出精准诊断。高质量的细胞学制片更是精准诊断的基础与关键,好的细胞蜡块离不开制作过程中的每一个环节,如浆膜腔积液的标准离心、去除红细胞等杂质、脱水、固定,包埋、切片、染色等,平时工作中一定要做好指控与对照,对降低假阳性率与假阴性率具有重要作用。随着细胞学技术的不断发展及患者需求的不断增加,免疫组化染色逐步应用于细胞学诊断中,使细胞学从传统的只依靠细胞学形态及医师诊断水平的经验诊断模式进入能够明确肿瘤来源及具体分类的精准诊断模式,很好地解决了细胞形态相似但组织来源不同的肿瘤和高分化肿瘤细胞与间皮细胞、炎性反应性增生细胞、多核巨细胞等的诊断及鉴别诊断。细胞蜡块具有可连续切片、保存时间长等优点,其切片具有细胞数量多、清晰,部分可形成相应组织学结构,且背景干净、长久保存等优点。
近几年来,我院病理科细胞蜡块免疫组化技术在学习与探索中日渐成熟,更好地满足了临床与患者的需求,开展例数逐渐增多,得到了临床与患者的一致好评,我们将再接再厉,在平稳中找不足,继续改进相关细节与环节,让细胞蜡块免疫组化诊断质量迈上一个新的台阶。
综上,细胞学标本不仅有创伤性小、安全、容易获得、患者容易接受的特点,而且出报告时间短,结果可靠,越来越受到临床的认可,尤其对肿瘤晚期无法获取手术标本的患者。目前,细胞蜡块已在有条件的医院被广泛用来基因检测,视为基因检测新的标本来源,具有一定的优势。
参考文献:
[1] Shivakumarswarmy U,Arakeri S U ,Karigowdar M H,et al.Diagnostic utility of the cell block method versus the conventional smear study in pleural fluid cytology[J].J Cytol,2012,29(1):11-15.
[2] 隋燕霞,柳雨,蒋娜,等.142例恶性胸水细胞蜡块的免疫组化检测及分子病理检测[J].临床与实验病理学杂志,2017,33(3):292-295.
[3] 刘芳,何欣,李晓琴.免疫组化标志物在鉴别浆膜腔积液恶性肿瘤细胞中的应用价值[J].临床与实验病理学杂志,2018,34(2):201-203.
[4] 宋艳芳,史晓兰,马青松.细胞蜡块技术在肿瘤诊断及分子分型中的应用价值[J].中华肿瘤防治杂志,2022,29(11):389-344.
[5] 陈琛.细胞蜡块结合免疫组化技术在胸腔积液中的诊断价值[J]肿瘤基础与临床,2021,34(03):261-163.
[6] Gomez-Fernandez C,Jorda M,Delgado Pl,et al.Thyroid transcription factor 1:a marker for lung adenoarinoma in body cavity fluids[J].Cancer,2022,96(5):189-293.
[7] Kimbrell HZ,Gustafson KS,Huang M,et al.Subclassification of nonsmall cell lung cancer bycytologic sampling:a logical approach with selective use of immunocytoche mistry[J].Acta Cytol,2012,56(4):419-424.
[8] 刘甜,刘嘉敏,陈意,等.细胞蜡块结合免疫组织化学、分子病理在胸腔积液病理诊断中的应用[J].诊断病理学杂志,2021,28(02),152-154.
[9]诊断细胞病理学/马正中等主编.-郑州:河南科学技术出版社,2000.5:832.
作者简介:1.王晓梅(出生年-1988年),学士,医师。2张慧智 主任医师。单位:甘肃省天水市第四人民医院病理科 邮编:741020